http://kimia-asyik.blogspot.com/2009/12/penentuan-entalpi-reaksi.html
1. Penentuan ∆H Reaksi berdasarkan Eksperimen (Kalorimeter)Penentuan kalor reaksi secara kalorimetris merupakan penentuan yang didasarkan atau diukur dari perubahan suhu larutan dan kalorimeter dengan prinsip perpindahan kalor, yaitu jumlah kalor yang diberikan sama dengan jumlah kalor yang diserap.
Kalorimeter adalah suatu sistem terisolasi (tidak ada pertukaran materi maupun energi dengan lingkungan di luar kalorimeter). Dengan demikian, semua kalor yang dibebaskan oleh reaksi yang terjadi dalam kalorimeter, kita dapat menentukan jumlah kalor yang diserap oleh air serta perangkat kalorimeter berdasarkan rumus :
q.larutan = m c ∆T
q.kalorimeter = C ∆T
q = jumlah kalor
m = massa air (larutan) di dalam kalorimeter
c = kalor jenis air (larutan) di dalam kalorimeter
C = kapasitas kalor dari kalorimeter
∆T = kenaikan suhu larutan (kalorimeter)
Oleh karena tidak ada kalor yang terbuang ke lingkungan, maka kalor
reaksi sama dengan kalor yang diserap oleh larutan dan kalorimeter,
tetapi tandanya berbeda :
qreaksi = -(qlarutan + qkalorimeter)
Kalorimeter yang sering digunakan adalah kalorimeter bom.
Kalorimeter bom terdiri dari sebuah bom (wadah tempatberlangsungnya
reaksi pembakaran, biasanya terbuat dari berlangsungnya reaksi
pembakaran, biasanya terbuat dari bahan stainless steel) dan sejumlah
air yang dibatasi dengan wadah kedap panas.
Jadi kalor reaksi sama dengan kalor yang diserap atau dilepaskan larutan,
sedangkan kalor yang diserap atau dilepaskan larutan, sedangkan kalor yang
diserap oleh gelas dan lingkungan diabaikan.
qreaksi = -qlarutan
2. Penentuan ∆H Reaksi dengan Hukum Hess
Hukum Hess : ” Kalor reaksi yang dilepas atau diserap hanya bergantung pada keadaan awal dan keadaan akhir”.
Untuk mengubah zat A menjadi zat B (produk) diperlukan kalor reaksi sebesar ∆H. Atau cara lain yaitu mengubah zat A menjadi zat B dengan kalor reaksi ∆H1, zat B diubah menjadi zat C dengan kalor reaksi ∆H2 dan zat C diubah menjadi zat D dengan kalor reaksi ∆H3 . Sehingga harga perubahan entalpi adalah
∆Hreaksi = ∆H1 + ∆H2 + ∆H3 .
Hal tersebut dapat dibuat siklus dan diagram tingkat energinya sebagai
berikut :

Siklus energi pembentukan zat D dari zat A

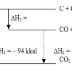
Diagram tingkat energi pembentukan zat D dari zat A
Contoh Soal :
Diketahui data entalpi reaksi sebagai berikut :
Ca(s) + ½ O2(g) → CaO(s) ∆H = - 635,5 kJ
C(s) + O2(g) → CO2(g) ∆H = - 393,5 kJ
Ca(s) + C(s) + ½ O2(g) → CaCO3(g) ∆H = - 1207,1 kJ
Hitunglah perubahan entalpi reaksi : CaO(s) + CO2(g) → CaCO3(s) !
Penyelesaian :
CaO(s) .............................→ Ca(s) + ½ O2(g) ....∆H = + 635,5 kJ
CO2(g)............................ → C(s) + O2(g) ............∆H = + 393,5 kJ
Ca(s) + C(s) + ½ O2(g) → CaCO3(s)................. ∆H = - 1207,1 kJ
_________________________________________ _
CaO(s) + CO2(g) ...........→ CaCO3(s).................. ∆H = - 178,1 kJ
3. Penentuan ∆H Reaksi Berdasarkan Data Perubahan Entalpi
Pembentukan Standar ( ∆Hof )
Cara lain perhitungan entalpi reaksi yaitu berdasarkan entalpi pembentukan standar( ∆Hof ) zat-zat yang ada pada reaksi tersebut.
∆Hreaksi = ∑∆Hof produk - ∑∆Hof reaktan
TABEL ENTALPI PEMBENTUKAN BEBERAPA ZAT| Zat | D | Zat | D |
| H2(g) | 0 | C2H4(g) | + 52,5 |
| O2(g) | 0 | CCl4(g) | - 96,0 |
| C(s) | 0 | NH3(g) | - 45,9 |
| H2O(g) | - 241,8 | NO2(g) | + 33,2 |
| H2O(l) | - 285,8 | SO2(g) | - 296,8 |
| CO2(g) | - 393,5 | HCl(g) | - 92,3 |
| CO(g) | -110,5 | NO(g) | + 90,3 |
Contoh Soal :
Dari tabel entalpi pembentukan diatas, tentukan :
a. ∆H reaksi pembakaran C2H4 !
b. Tentukan jumlah kalor yang dibebaskan pada pembakaran 56 g gas C2H4
a. Reaksi pembakaran C2H4
C2H4(g) + 3 O2(g)→2CO2(g) + 2H2O(l)
∆H reaksi = ∆Hof hasil reaksi - ∆Hof pereaksi
= ( 2. ∆Hof CO2 + 2. .∆Hof H2O ) – ( 1. ∆HofC2H4 + 3. ∆Hof O2)
= ( 2 . -393,5 + 2. -285,8 ) – ( 1. 52,5 + 3. 0 )
= -787 – 571,6 + 52,5
= - 1306,1 kJ/mol
b. Mr C2H4 = (2x12) + (4x1) = 28
Mol C2H4 = 56/28 = 2 mol
∆H pembakaran 2 mol C2H4 = 2 mol x ( -1306,1 kJ/mol )
= -2612,2 kJ
Jadi pada pembakaran 56 gram gas C2H4 dibebaskan kalor sebesar
2612,2 kJ
4. Penentuan ∆H Reaksi Dari Energi Ikatan
Reaksi kimia antarmolekul dapat dianggap berlangsung dalam 2 tahap
yaitu :
I. Pemutusan ikatan pada pereaksi
II.Pembentukan ikatan pada produk
Misal, pada reaksi antara gas klorin dengan gas hidrogen membentuk gas
hidrogen klorida dapat digambarkan sebagai berikut :

∆H tahap-I = ∑ Energi ikatan pada pereaksi (yang putus)
∆H tahap-II = -∑ Energi ikatan pada produk (yang terbentuk).
∆H reaksi = ∑ Energi ikatan pereaksi yang putus - ∑ Energi ikatan produk yang terbentuk
= ∑ Eruas kiri - ∑ Eruas kanan
TABEL ENERGI IKATAN
| Ikatan | E (kJ/mol) | Ikatan | E (kJ/mol) |
| H-H | 436 | O=O | 498 |
| H-C | 415 | C≡N | 891 |
| H-N | 390 | F-F | 160 |
| C-C | 345 | Cl-Cl | 243 |
| C≡C | 837 | H-Cl | 432 |
| C-O | 350 | C=C | 611 |
| C=O | 741 | I-I | 150 |
| C-Cl | 330 | N=N | 418 |
| O-H | 450 | C-F | 485 |
Penyelesaian :
........H
.........l
H – C – O-H +1 ½ O=O → O=C=O +2H-O-H
........l
.......H
∆H reaksi = ∑Epemutusan -∑Epembentukan
= { (3.Ec-H)+( 1.EO-H) +(1.EC-O)+ (1 ½ EO=O)} – {(2.EC=O)
+(4.EO-H)}
= {(3.415)+(1.460)+(1.350)+1 ½.498)} –{(2.741)+(4.460)}
= 2802-3322
= -520 kJ/mol
0 Comments:
Langganan:
Posting Komentar (Atom)

 Ikatan Hidrogen dan ikatan Van der Waals Gaya antarmolekul adalah gaya elektromagnetik yang terjadi antara molekul atau antara bagian y...
Ikatan Hidrogen dan ikatan Van der Waals Gaya antarmolekul adalah gaya elektromagnetik yang terjadi antara molekul atau antara bagian y...
 http://kimia-asyik.blogspot.com/search/label/Soal-Soal Soal Ulangan Hidrokarbon 1. Tentukan jumlah atom C primer, sekunder, tersie...
http://kimia-asyik.blogspot.com/search/label/Soal-Soal Soal Ulangan Hidrokarbon 1. Tentukan jumlah atom C primer, sekunder, tersie...
 Kimia inti adalah kajian mengenai perubahan-perubahan dalam inti atom. Perubahan ini disebut reaksi inti. Peluruhan radioaktif dan t...
Kimia inti adalah kajian mengenai perubahan-perubahan dalam inti atom. Perubahan ini disebut reaksi inti. Peluruhan radioaktif dan t...
 Kelompok Bajak Laut Topi Jerami adalah kelompok bajak laut fiktif yang ada dalam cerita manga dan anime One Piece . kelompok bajak l...
Kelompok Bajak Laut Topi Jerami adalah kelompok bajak laut fiktif yang ada dalam cerita manga dan anime One Piece . kelompok bajak l...
 http://kimia-asyik.blogspot.com/2010/01/hidrolisis-garam.html Reaksi asam dan basa menghasilkan garam. Asam terdiri dari asam kuat dan as...
http://kimia-asyik.blogspot.com/2010/01/hidrolisis-garam.html Reaksi asam dan basa menghasilkan garam. Asam terdiri dari asam kuat dan as...






